Пояснительная записка.
Химия считается наиболее трудной школьной дисциплиной. В настоящее время под лозунгом гуманитаризации обучения происходит сокращение учебных планов в области естествознания. При этом забывается, что химия, как наука, занимая одно из центральных положений в естествознании, составляет основу для формирования научного мировоззрения учащихся. Главной проблемой в преподавании химии является перегруженность курса химии основной школы в связи с переходом на концентрическую систему. Актуальность данной проблемы возрастает в связи с тем, что химические знания необходимы каждому человеку, они определяют рациональное поведение человека в окружающей среде, необходимы в повседневной жизни; элективные курсы и курсы по выбору будут, в какой-то степени, решать те задачи, которые на уроках химии не удается решить в полном объёме из-за дефицита времени.
Решить эту проблему можно с помощью курса по выбору или пропедевтического курса. Необходимость введения предлагаемого курса вызвана несколькими причинами. В частности, это сложность программного материала, сокращение количества учебных часов, уменьшение химического эксперимента на уроках, а также искаженные знания школьников, почерпнутые из средств массовой информации ещё до знакомства с предметом.
В нашей школе имеется возможность ввести пропедевтический курс изучения химии в 7 классе один час в неделю за счет национального – регионального компонента. Данный курс дает первоначальные понятия о большинстве разделов химии, не предполагая их основательного изучения.
Особенность изучаемого курса состоит в том, что изучение первоначальных химических понятий на год раньше дает возможность разгрузить достаточно сложную по содержанию, с большим объемом учебной информации программу по химии в 8-м классе. Учащимся предоставляется время для привыкания к химическому языку, химической символике, приобретения практических умений, что способствует более осмысленному использованию ими ключевых понятий и выработке экспериментальных навыков в 8-м классе. Кроме того, в 8-м классе освобождаются часы на более тщательное и глубокое рассмотрение материалов таких разделов, как «Обобщение сведений о важнейших классах неорганических соединений», «Периодический закон и периодическая система химических элементов Д.И.Менделеева», «Строение атома». В 7-ом классе школьники приобретают умение решать простые расчетные задачи по химическим формулам, поэтому в 8-ом классе у учителя появляется возможность увеличить количество часов на приобретение умений решать другие типы расчетных задач: вычисление объемов газов (при н.у.); расчеты по химическим уравнениям.
В соответствии с требованиями Государственного образовательного стандарта в курсе подчеркивается, что химия – наука экспериментальная. Поэтому в 7-ом классе рассматриваются такие методологические понятия учебного предмета, как эксперимент, наблюдение, описание, моделирование, гипотеза, вывод. Хорошо подобранные опыты позволяют отразить связь теории и эксперимента. Химический эксперимент должен быть нацелен на приобретение навыков, которые можно использовать в реальной жизни (разделение смесей, приготовление раствора с заданной массовой долей растворенного вещества, нейтрализация кислоты и щелочи). Большое внимание уделяется практическим работам, которые позволяют привить не только важные практические умения, но и развивать самостоятельность учащихся, их познавательную деятельность. Часть работ носит исследовательский характер (выращивание кристаллов поваренной соли, наблюдение за горящей свечой).
Данный образовательный курс является источником знаний, позволяет полнее учесть интересы учащихся, следовательно, сделать изучение предмета более интересным, соответственно, получить более высокие результаты обучения.
Данный курс знакомства с химией в 7 классе совпадает по времени с изучением тех же понятий в курсе физики, и это способствует более глубокому усвоению материала. Кроме этого, в этом курсе используется материал, связанный с биологией.
Данная программа рассчитана на 34 часа и адресована учащимся 7 класса средней общеобразовательной школы, но частично может использоваться при изучении химии в 8 классе при повторении, а именно та часть, где изучаются химические расчеты.
Общими принципами отбора содержания материала программы являются:
- системность;
- целостность;
- объективность;
- научность;
- доступность для учащихся основной школы;
- реалистичность;
- практическая направленность.
Курс проводится в виде лекционно – практических уроков с оформлением содержания занятия в рабочих тетрадях и «Портфолио ученика».
Данная программа является авторской и построена в соответствии с требованиями Закона РФ «Об образовании», Государственного образовательного стандарта по химии, Устава школы, инструкций по ТБ.
В результате прохождения программного материала обучающийся должен знать:
- химический язык (знаки химических элементов);
- применение некоторых веществ;
- ТБ при работе с химическими веществами.
Уметь:
- писать, называть знаки химических элементов;
- различать простые и сложные вещества;
- составлять простейшие химические формулы;
- выполнять простейшие расчеты по химическим формулам;
- наблюдать, описывать, сравнивать, анализировать, моделировать химические процессы;
- выполнять простейший химический эксперимент;
- выдвигать гипотезы, делать выводы;
- соблюдать правила ТБ при работе с веществами на уроке и в домашних условиях.
В соответствии с этим, целью прохождения курса является:
- подготовить учащихся к изучению серьезного учебного предмета;
- разгрузить, насколько это возможно, курс химии основной школы;
- сформировать устойчивый познавательный интерес к химии.
В ходе её достижения решаются задачи:
- сформировать знания о химическом языке через знакомство с некоторыми химическими элементами;
- отработать те предметные умения, навыки (в первую очередь для проведения эксперимента, для решения расчетных задач по химии), на которые не хватает времени при изучении химии в 8 и 9 классах;
- показать яркие, занимательные, эмоционально насыщенные эпизоды становления и развития химии, которые учитель почти не может себе позволить при вечном недостатке времени;
- изучить свойства некоторых веществ, часто применяемых в домашних условиях;
- начать работу по формированию коммуникативной компетенции.
Усвоение материала можно проследить через отчеты по практическим работам, самостоятельные творческие работы, анкетирование, тесты; итоги работы подводятся на последнем занятии в виде защиты рефератов.
В структуре изучаемой программы выделяются следующие основные темы:
Предмет химии и её история.
-
Вещество.
-
Химические реакции.
-
Экспериментальные основы химии.
Первая тема «предмет химии и её история» знакомит учащихся с сущностью предмета, историей формирования химии как науки.
Вторая тема «Вещество» - самая объемная и насыщенная, продолжает межпредметную интеграцию с физикой, биологией, формируя устойчивое представление о веществах простых и сложных, о частицах вещества (атомах, ионах, молекулах), основных характеристиках веществ в твердом, жидком и газообразном состоянии. Дается представление о физических явлениях. Учащиеся получают знания о химических элементах и простых веществах ими образованных, применение их человеком с древних времен и до наших дней. Здесь учащиеся знакомятся с простейшими химическими расчетами по формулам веществ, со смесями и способами их разделения.
Третья тема «Химические реакции» содержит информацию о химических явлениях и дает представление о методологии познания окружающей природы в системе естественных наук.
В четвертой теме «Экспериментальные основы химии» у учащихся формируются практические навыки по работе с химическим оборудованием, веществами, соблюдением ТБ.
Заканчиваетя изучение химии в 7 классе итоговым уроком, на котором учащиеся защищают свои творческие работы по этому курсу.
Ожидаемые результаты изучения данного кура: формирование устойчивого интереса к изучаемому предмету, умение обращаться с веществами в быту, приобретение первоначальных знаний по химии.
Для поддержания интереса к занятиям и обеспечения доступности изучаемого материала, для преодоления трудностей первого периода формирования экспериментальных умений (в 7-ом и 8-ом классах) используется интерактивная доска.
Цель использования ИД: рационализировать формы преподнесения информации; повысить степень наглядности; активизировать познавательную деятельность учащихся.
Результатом работы с ИД должно стать повышение качества образования, соответствующего современным требованиям к общему образованию.
При использовании ИД на уроках химии учащиеся довольно быстро выучили знаки химических элементов. Если на обычных уроках на это затрачивается 4 – 5 уроков и знаки усваивались учащимися на 81%, то при изучении химии с использованием ИД, уже на втором уроке почти все дети запомнили знаки, а на третьем уроке их знали даже слабоуспевающие ученики (98%).
В нынешнем году учащиеся 8-го класса, которые изучали химию в 7-ом классе, дают более высокие результаты (качество знаний 81%) по сравнению с предыдущими восьмиклассниками - 77% по итогам I четверти. Интерес к химии у нынешних восьмиклассников гораздо выше, работают они на уроках активнее, даже слабоуспевающие ученики.
Итак, введение пропедевтического курса по химии в 7 классе дает положительный результат при дальнейшем изучении этого предмета.
Тематический план.
№ |
Название темы |
Дата |
Виды деятельности |
Основное содержание урока |
I |
Предмет химии и её история |
|
|
|
1 |
Предмет химии |
сентябрь |
Лекция |
Химия – наука о веществах, их свойствах и превращениях. |
2 |
История развития химии как науки |
сентябрь |
Лекция |
Химия в древности (алхимия), развитие химии в XIX в., химия в наши дни |
II |
Вещество |
|
|
|
3 |
Вещества. Простые и сложные вещества |
сентябрь |
Беседа, работа на ИД |
Тело и вещество. Вещества сложные и простые. |
4 |
Превращение веществ. Роль химии в нашей жизни |
сентябрь |
Беседа, дискуссия |
Физические свойства веществ. Химические свойства веществ. Для чего мы изучаем химию? |
5 |
Периодическая система химических элементов. Химический язык |
октябрь |
Лекция |
Структура таблицы Д.И.Менделеева: периоды, группы. Информация, которую несут знаки химических элементов. |
6-9 |
Химические элементы и вещества вокруг нас (азот, алюминий, железо, золото, водород, вода, хлорид натрия, карбонат кальция) |
октябрь- ноябрь |
Использование мультимедийной презентации |
Простые (азот, алюминий, железо, золото, водород) и сложные (вода, хлорид натрия, карбонат кальция) вещества, их состав, встречаемость в природе и применение. |
10 |
Химические формулы. Относительная атомная и молекулярная массы |
ноябрь |
Беседа, работа на ИД |
Информация, которую несут химические формулы. Относительная атомная и молекулярная массы. |
11 |
Расчеты по химическим формулам. Количество вещества – моль |
ноябрь |
Лекция, беседа |
Моль – это количество вещества, которое содержит 6.10 23молекул этого вещества |
12-14 |
Решение задач с использование понятия «моль» |
декабрь |
Решение задач |
Решение задач на нахождение молярной массы, числа молекул в определенном количестве вещества. |
15 |
Зачет по решению задач |
декабрь |
Самостоятельная работа |
Решение задач |
16 |
Простые вещества металлы. Использование металлов человеком |
январь |
Использование мультимедийной презентации |
Век медный, бронзовый, железный. Физические свойства металлов. |
17 |
Простые вещества неметаллы. Использование неметаллов человеком |
январь |
Использование мультимедийной презентации |
Физические свойства неметаллов. Отличительные черты неметаллов от металлов. Понятие «аллотропия». Применение неметаллов. |
18 |
Явления, происходящие с веществами |
январь |
Беседа, работа на ИД |
Явления физические и химические. Примеры физических и химических явлений, известных учащимся. |
19 |
Чистые вещества и смеси. Разделение смесей. |
февраль |
Беседа. Лабораторные опыты. |
Примеры чистых веществ и смесей. Отличие смесей от химических соединений. Приемы разделения смесей: растворение, фильтрование, отстаивание, действие магнитом. Разделение смесей в домашних условиях, в походе. |
20 -21 |
Массовая доля вещества в растворе |
февраль |
Решение задач, лабораторные опыты |
Вычисление массовой доли вещества в растворе. Методика приготовления раствора с заданной массовой долей растворенного вещества |
22 |
Контрольная работа по теме «Вещество» |
февраль |
Решение тестов |
|
III |
Химические реакции |
|
|
|
23 |
Химические реакции. Условия протекания и прекращения химических реакций. Признаки химических реакций. |
март |
Беседа, лабораторные опыты |
Особенности химических реакций, отличие их от физических явлений. Условия протекания и прекращения химических реакций. |
24 |
Реакции, которые происходят вокруг нас. |
март |
Беседа |
Изменения пищевых продуктов при неправильном хранении. Как нейтрализовать действие уксусной кислоты и гашеной извести. |
25 |
Фотосинтез. |
март |
Лекция с элементами беседы |
Реакции, происходящие при фотосинтезе. Значение реакций фотосинтеза |
26 |
Реакции горения. Коррозия |
апрель |
Беседа |
Реакции горения в быту и в химии. Коррозия металлов, химизм реакции коррозии. Как уберечь металлы от коррозии. |
27 |
Качественные реакции в химии |
|
Лабораторные опыты |
Действие индикаторов на уксусную кислоту, раствор гашеной извести, раствор питьевой соды. |
28 |
Зачет по теме «Химические реакции» |
апрель |
Письменная контрольная работа |
|
|
Экспериментальные основы химии |
|
|
|
29 |
Знакомство с химическим оборудованием. Правила ТБ |
апрель |
Практическая работа |
Знакомство с лабораторным штативом, держателем пробирок, пробирками. Правила ТБ при выполнении практических работ |
30 |
Наблюдение за горящей свечой. Устройство и работа спиртовки. |
апрель |
Практическая работа |
Разделение смеси речного песка и поваренной соли. |
31 |
Разделение смесей |
май |
Практическая работа |
Приготовление раствора поваренной соли с заданной массовой долей растворенного вещества |
32 |
Приготовление раствора с заданной массовой долей растворенного вещества |
май |
Практическая работа |
Знакомство с методикой выращивания кристаллов поваренной соли. Выращивание кристаллов поваренной соли |
33 |
Выращивание кристаллов поваренной соли |
май |
Практическая работа |
Наблюдение за горящей свечой. Устройство и работа спиртовки. |
34 |
Итоговый урок. Защита рефератов |
май |
Отчет учащихся о проделанной работе |
Учащиеся отчитываются о работе за год |
Содержание курса.
Тема 1. Предмет химии и её история (2 ч.)
Что изучает химия. Египет – родина химии. Современная химия, её положительное и отрицательное значение в жизни современного общества.
Тема 2. Вещества. (20ч.)
Вещества простые и сложные. Превращение веществ, их рол в жизни современного человека. Свойства веществ как основа их применения. Физические свойства веществ и физические явления, агрегатное состояние вещества. Структура периодической системы химических элементов Д.И.Менделеева. Химические элементы. Химический элемент как определенный вид атомов. Химические знаки. Информация, которую несут химические знаки и формулы. Химические элементы и простые вещества вокруг нас. Химические формулы, относительная атомная и молекулярная масса. Количество вещества – моль. Расчеты по химическим формулам (массовая доля элемента в сложном веществе) и с использованием понятия «моль». Простые вещества металлы и неметаллы, их использование человеком. Сравнение свойств металлов и неметаллов. Чистые вещества и смеси, разделение смесей.
Демонстрации. 1. Коллекции физических тел из одного вещества (стеклянной лабораторной посуды). 2. Коллекция «Свойства алюминия как основа его применения». 3. коллекция «Металлы». 4. Коллекция «Неметаллы». 5. Переходы воды в различные агрегатные состояния. 6. Коллекция природных и бытовых смесей различных агрегатных состояний (природные и бытовые растворы, средства бытовой химии и гигиены). 6. Коллекция стекол и сплавов. 7. Диаграмма состава воздуха. 8. Образцы химических препаратов с указанием степени их чистоты. 9. Аптечные и пищевые растворы с указанием их состава. Разделение порошков серы и железа.
Тема 3. Химические реакции. (6 ч.)
Химические явления и химические реакции. Признаки химических реакций (изменение окраски, появление запаха, выделение газа, выделение или поглощение тепла, выпадение осадка). Условия протекания и прекращения химических реакций (соприкосновение веществ, растворение, измельчение, доступ кислорода при горении). Изменения, которые происходят с пищевыми продуктами при неправильном хранении. Нейтрализация действия уксусной кислоты раствором питьевой соды, и гашеной извести – раствором борной кислоты. Фотосинтез – химическая реакция, происходящая в зеленых растениях, её значение для живой природы. Реакции горения, их значение для человека. Коррозия – пример реакции неполезной для человека. Качественные реакции в химии: действие уксусной кислоты и питьевой соды на индикаторы химические и природные.
Демонстрация. 1. Обугливание сахара и бумаги концентрированной серной кислотой. 2. Выпадение осадка гидроксида меди. 3. Взаимодействие питьевой соды с уксусной кислотой. 4. Тепловой эффект при разбавлении серной кислоты. 5. Понижение температуры при растворении в воде калийной селитры. 6. Помутнение известковой воды при взаимодействии с углекислым газом. 7. Коллекция разновидностей кальцита – различных видов мела, мрамора, известняка. 8. Коррозия железного гвоздя в разных условиях.
Тема 4. Экспериментальные основы химии. (6 ч.)
Знакомство с химическим оборудованием (химической посудой, держателем, спиртовкой, лабораторным штативом). Техника безопасности при работе с химическими веществами. Разделение смеси поваренной соли и речного песка. Приготовление раствора поваренной соли заданной концентрации. Выращивание кристаллов поваренной соли. Наблюдение за горящей свечой. Работа со спиртовкой. Определение зон пламени свечи и спиртовки.
Защита творческих работ по итогам года.
Практические работы. 1. Знакомство с химическим оборудованием. Правила ТБ. 2. Наблюдение за горящей свечой. Устройство и работа спиртовки. 3. Разделение смесей 4. Приготовление раствора с заданной массовой долей растворенного вещества. 5. Выращивание кристаллов поваренной соли.
Аннотация.
Третьякова Екатерина Григорьевна, учитель химии и биологии, МОУ «Сухановская СОШ», ВКК.
Представлена рабочая программа по пропедевтическому курсу по химии в 7 классе «Введение в химию».
Цель: показать достигнутые результаты инновационной деятельности.
Задачи: представить программу пропедевтического курса изучения химии в 7 классе, разработки уроков по данному курсу; использование ИКТ при изучении данного курса.
Данная программа является авторской и разработана для учащихся 7 класса. Необходимость введения курса в 7 классе вызвана перегруженностью изучаемого материала в курсе 7 – 8 классов, сокращением учебных часов, искажение знаний школьников, почерпнутые из средств массовой информации еще до знакомства с предметом.
Особенностью изучаемого курса является то, что изучение первоначальных химических понятий на год раньше дает возможность разгрузить достаточно сложную по содержанию, с большим объемом учебной информации программу по химии в 8 классе.
Программа рассчитана на 34 часа и адресована учащимся 7 класса.
Курс проводится в виде лекционно – практических уроков с оформлением содержания занятия в рабочих тетрадях и «Портфолио учащегося».
Целью прохождения курса является: - подготовить учащихся к изучению серьезного учебного предмета; разгрузить, насколько это возможно, курс химии основной школы; сформировать устойчивый познавательный интерес к химии.
В ходе её достижения решаются задачи: сформировать знания о химическом языке через знакомство с некоторыми химическими элементами; отработать те предметные умения, навыки, на которые не хватает времени при изучении химии в 8, 9 классах; изучить свойства некоторых веществ, часто применяемых в домашних условиях; начать работу по формированию информационно – коммуникативной компетенции.
Усвоение материала можно проследить через отчеты по практическим работам, тесты; итоги подводятся на последнем занятии в виде защиты реферата.
В структуре изучаемой программы выделяются следующие основные темы:
-
Предмет химии и её история. Здесь происходит знакомство с сущностью предмета, историей формирования химии как науки.
-
Вещество. В этой теме учащиеся знакомятся с веществами простыми и сложными, частицами (атомами, молекулами), основными характеристиками вещества. Учащиеся получают знания о применении веществ человеком; учатся выполнять несложные химические расчеты.
-
Химические реакции. Эта тема содержит информацию о химических явлениях и дает представление о методологии познания окружающей природы в системе естественных наук.
-
Экспериментальные основы химии. У учащихся формируются практические навыки по работе с химическим оборудованием, веществами, соблюдением ТБ.
Ожидаемые результаты: формирование устойчивого интереса к изучаемому предмету, приобретение первоначальных знаний по химии, умение обращаться с веществами в быту, критически относиться к различного рода химической информации.
Для поддержки интереса к занятиям и обеспечения доступности изучаемого материала, для преодоления трудностей первого периода формирования экспериментальных умений использую интерактивную доску. Результатом работы на ИД является повышение качества образования, соответствующего современным требованиям к общему образованию. При использовании ИД учащиеся довольно быстро учат знаки химических элементов, начинают различать простые вещества и сложные.
Введение пропедевтического курса по химии в 7 классе дает положительный результат при дальнейшем изучении химии.
К программе прилагаются разработки уроков и материал, используемый на ИД.
Тема урока «Чистые вещества и смеси»
Тип урока: формирование новых знаний.
Цель: сформировать представление о чистых веществах и смесях, способах разделения смесей.
Задачи:
Образовательные:
-
Изучить отличия чистых веществ и смесей;
-
Изучить классификацию смесей;
-
Изучить некоторые способы разделения смесей на основании свойств чистых веществ, составляющих смеси;
Развивающие:
-
Формирование приемов умственной деятельности: анализ, синтез, сравнение, обобщение;
-
Развивать умение правильно наблюдать и делать выводы из наблюдений;
Воспитательные:
Результативность урока.
Учащиеся узнают:
- чем отличаются чистые вещества от смесей;
- что свойства чистого вещества в смеси сохраняются;
- чтобы выделить чистое вещество из смеси, нужно знать его свойства
- для чего нужно разделять смеси.
Учащиеся научатся:
- способам разделения смесей.
Методы, используемые на уроке: эвристическая беседа.
Оборудование: воронка, фильтр, химические стаканчики, магнит, делительная воронка, фарфоровая чашка, лабораторный штатив, спиртовка, таблетки активированного угля, сплавы металлов, горные породы, уксусная кислота, молоко, поролон, пористый шоколад, лимонад, аэрозольный баллон, смеси серы и железных опилок, воды и растительного масла, речного песка и воды, воды и поваренной соли.
План урока.
I этап. Актуализация знаний и мотивация на усвоение нового материала.
- Что изучает химия? (вещества)
- Какие мы знаем вещества? (простые и сложные)
Но вещества могут существовать не только в чистом виде, но и смешиваться друг с другом.
Тема нашего урока «Чистые вещества и смеси»
II этап. Изучение нового материала.
Много ли в природе чистых веществ? Приведите примеры. Дети называют, но таких веществ оказывается немного, и они приходят к выводу, что большинство веществ являются смесями, приводят примеры смесей.
Что означает слово «смесь»? (слово это произошло от слова «смешивать», «перемешивать»).
Смесь состоит из двух и более компонентов, находящихся в непосредственном контакте друг с другом (определение записываем в тетрадь).
Докажите, что воздух, молоко, морская вода являются смесями (учащиеся перечисляют вещества, которые входят в состав смесей).
Смеси.
Однородные Неоднородные
(растворы поваренной соли, (смесь железных и медных
сахара в воде ) опилок, глина с водой)
Назовите отличие чистых веществ и смесей.
Учащиеся делают вывод, что чистые вещества состоят из частиц одного вещества, а смеси – из частиц разных веществ.
Проблема – изменяют ли свои свойства вещества, если они содержатся в смеси? (Пример: сахар – твердое вещество и сахар в растворе).
Учащиеся после обсуждения проблемы приходят к выводу: вещества в смесях своих свойств не изменяют.
Обладают ли смеси теми же свойствами, что и вещества их образующие?
Чистая вода кипит при 100С и замерзает при 0С, а морская вода замерзает при -1,9С. Чем это вы можете объяснить? (В состав морской воды входят соли).
Всем известно, что алюминий пластичный металл. А в прошлом веке считали, алюминий трудно вытянуть в проволоку и прокатать в тонкие листы. Как оказалось, в то время имели дело не с чистым металлом, а с металлом, загрязненным примесями. Хром считали хрупким металлом, пока не выделили из него примеси, и он стал пластичным.
Чистые вещества – это вещества с постоянными физическими свойствами. Современные химики научились получать особо чистые вещества, которые применяются в атомной энергетике, полупроводниковой промышленности, медицине.
А как выделить чистое вещество из смеси?
Вспомним сказку про Золушку. Поехала мачеха с дочерями на бал, а Золушке дала приказание разобрать крупу. По каким признакам Золушка разделяла смесь круп? На основе чего было это разделение?
Какие способы разделения смесей используют в химии? Проанализируйте состав смесей и предложите способ их разделения: речной песок и вода, вода и растительное масло, вода и поваренная соль, медные и железные стружки? (Фильтрование, отстаивание, выпаривание).
III этап. Закрепление.
Учащиеся под руководством учителя проделывают несложные опыты по разделению смесей.
1 группа - речной песок и вода
2 группа - вода и растительное масло
3 группа – вода и поваренная соль
4 группа – медные и железные опилки
После завершения работы представители каждой группы отчитываются о проделанных опытах.
IV этап. Домашнее задание. Придумать примеры смесей и способы их разделения. Сделать соответствующие записи в тетради.
V этап. Итоги урока. Рефлексия. Выразить свое отношение к уроку 1-2 словами.
Практическая работа
по теме «Выращивание кристаллов поваренной соли».
Тип урока - применение знаний на практике.
Цель: расширить у учащихся представление о растворах, сформировать умение работать с насыщенными растворами.
Задачи урока.
Образовательные:
-
Углубить знания о растворах;
-
Научить приемам выращивания кристаллов из насыщенного раствора;
-
Продолжить формирование умений учащихся по работе с лабораторным оборудованием;
Воспитательные:
-
Вовлечь в активную практическую деятельность;
-
Совершенствовать навыки общения;
-
Воспитывать культуру поведения при проведении практических занятий;
Развивающие:
-
Развивать умение проводить, наблюдать, описывать эксперимент на примере выращивания кристаллов;
-
Развивать логическое мышление.
Методы обучения: продуктивные, исследовательские.
Результативность урока:
Учащиеся узнают:
- о насыщенных и ненасыщенных растворах;
- методику выращивания кристаллов.
Учащиеся научатся:
- готовить насыщенные растворы;
- выращивать из них кристаллы.
Оборудование: поваренная соль, воронка, бумажный фильтр, спиртовка, спички, лабораторный штатив с кольцом, асбестовая сетка, стеклянные стаканы, стеклянная палочка, нитка.
Ход урока
1 Этап. Правила техники безопасности при работе в кабинете химии на практической работе.
-
Строго выполнять указанные учителем меры предосторожности, иначе может произойти несчастный случай.
-
Не пробовать вещества на вкус.
-
Твердые вещества брать только сухой ложкой.
-
Нагревать раствор осторожно, поставив стакан на асбестовую сетку.
-
Перемешивать жидкость палочкой осторожно, не задевая стенок стакана.
-
Раствор при фильтровании наливать в воронку по палочке.
-
Обращаться бережно с посудой.
- Закончив работу, приведите рабочее место в порядок.
2 Этап. Инструкция по приготовлению насыщенного раствора поваренной соли.
Рассмотрим таблицу растворимости поваренной соли при разных температурах.
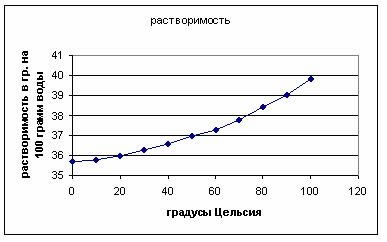
Таблица растворимости поваренной соли при разной температуре
Готовим насыщенный раствор соли в горячей (70 – 80С) дистиллированной воде, т.к. хотя растворимость соли не очень сильно меняется при изменении температуры (см. Таблицу), но всё же при охлаждении более горячей воды возникнет большее пресыщение. (Можно раствор поместить в термос, он будет охлаждаться медленнее и кристаллы будут расти равномернее.) Раствор отфильтровали и поместили в него шелковую нить с узелками. Если взять нить другого типа, то соль, поднимаясь по её капиллярам вместе с раствором, будет кристаллизоваться преимущественно на стержне, на который крепится нить. Первые кристаллы появились на поверхности и имели форму воронок. Это связано с тем, что при быстрой кристаллизации, кристаллу легче расти ребрами и гранями. Такие кристаллы называются скелетными. Скопление прозрачных воронок плавало, а потом они тонули и на дне зарастали, мутнели и белели, и превращались в правильные кубики. На стенке сосуда выросли дендриты соли, похожие на ледяные узоры на окнах. Дендрит – это отложения различных минералов, по форме напоминающие растения. Это сростки скелетных кристаллов. Там, где перенасыщение было больше всего, соль образовывает соляные своды над поверхностью раствора. Несколько разных по мощности сводов не только показывали, на каком уровне раствор стоял дольше всего, но и саму скорость испарения раствора. Дендриты растут из скелетных кристаллов. Дело в том, что при высоких перенасыщениях кристаллу выгодней расти ребрами и вершинами, а не гранями. Наибольшее перенасыщение возникает на поверхности рассола, где сильнее всего испарение. А на шелковой нити выросли правильные кубические кристаллы.
Можно увеличить размер кристаллов. Для этого достаем нить из раствора, оставляем один – два крупных кристалла и переносим ее в новый насыщенный раствор. Если это повторять несколько раз, то можно вырастить красивые крупные кубические кристаллы.
3 Этап. Приготовление раствора.
4 Этап Оформление работы в тетради.
Записи в тетради:
| Что делаю
|
Что наблюдаю |
Растворяю соль в воде |
В холодной воде получил насыщенный раствор (на дне стакана – кристаллы соли) |
Нагреваю раствор |
Кристаллы растворились |
Добавляю ещё соли |
До получения насыщенного раствора понадобилось немного соли |
Фильтрую раствор |
Получаю прозрачный раствор |
Опускаю шелковую нить в горячий раствор |
На нити и на стенках стакана через некоторое время появляются кристаллы соли кубической формы (на нити) |
Готовлю новый насыщенный раствор и переношу туда нить |
Кристаллы увеличиваются в размерах |
|
|
5 Этап. Выводы по работе.
6 Этап. Рефлексия.
Чему вы научились на уроке? Нужно ли это вам?
7 Этап. Приводим рабочее место в порядок.
Контрольная работа
по теме «Химические реакции»
Тип урока: урок контроля и проверки знаний и умений.
Форма урока: контрольная работа.
Цель: осуществить контроль обучения, выявить уровень усвоения материала, сформированности умений и навыков.
Задачи.
Образовательные:
-
Выявить качество и уровень овладения знаниями и умениями, полученными на уроках;
-
Обобщить материал как систему знаний, проверить способность к творческому мышлению и самостоятельной деятельности;
Воспитательные:
-
Способствовать формированию ответственного отношения к учению;
-
Воспитывать культуру учебного труда, экономного расходования времени;
Развивающие:
-
Развивать логическое мышление, память, способность к анализу и синтезу;
-
Формировать навыки самоконтроля.
Вопросы для контрольной работы:
На оценку «3» выполнить задания:
1. Какие явления называются химическими? Приведите примеры химических явлений, которые происходят в быту.
2. Опишите реакцию взаимодействия железа с серой. Какие необходимы для этого условия?
3. Назовите признаки химических реакций. Приведите примеры.
На оценку «4» выполнить предыдущие задания и следующие:
4 .Докажите, что горение дров – это химическая реакция. Почему при закрытой печке дрова не горят?
5. К каким явлениям вы отнесете горение свечи и электрической лампочки? Дайте подробное объяснение.
На оценку «5» выполнить задания под № 1- 5 и следующие задания:
6. Под действием кислотных дождей разрушаются мраморные скульптуры. Какое явление происходит при этом, каковы признаки этого явления? Ваше отношение к этому явлению.
Задания учащимся выдаются на индивидуальных карточках.

